환자단체연합회, 5년간 등재된 항암제 및 희귀질환치료제 분석
"정부 약속한 신속등재-사후평가 체계 서둘러야"
식품의약품안전처 허가 이후 건강보험 적용까지 항암제는 평균 1년 10개월, 희귀질환 치료제는 평균 2년 11개월이 소요된다는 결과가 나왔다. 한국환자단체연합회가 암·희귀질환 환자의 신약 접근성을 점검하기 위해 건강보험 등재 기간을 분석한 결과 이 같이 나타났다. 환자단체는 정부가 '신속등재-사후평가 관리체계'를 조속히 구축·추진해야 한다고 촉구했다.
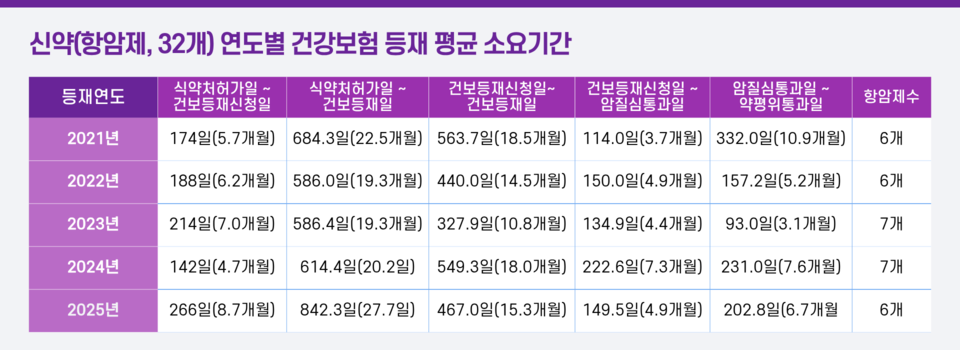
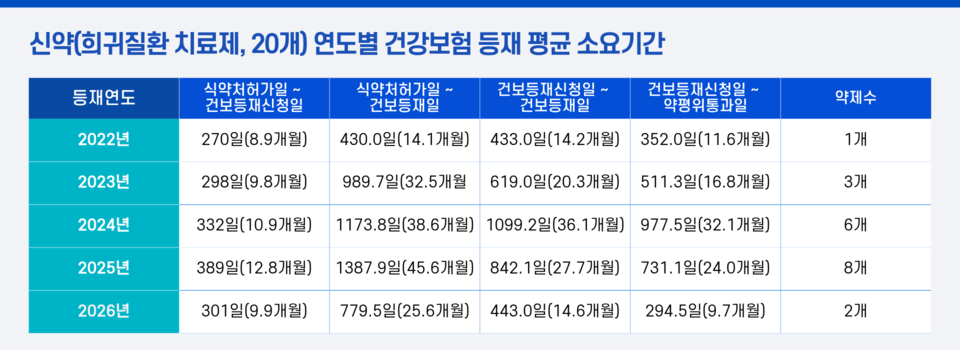
10일 환자단체연합회는 2021~2025년 5년간 건강보험에 등재된 항암제 32개, 2022~2025년 4년간 등재된 희귀질환 치료제 20개를 대상으로 식약처 허가 이후 건강보험 등재까지 소요 기간을 분석했다고 밝혔다.
현행 신약 등재 절차는 식약처 허가 후 제약사의 등재 신청을 시작으로 건강보험심사평가원의 급여 적정성 평가, 국민건강보험공단 약가 협상, 보건복지부 건강보험정책심의위원회 심의 및 고시를 거쳐 최종 결정된다.
연합회는 심평원의 급여 적정성 평가가 처리 기간 120일(최대 150일)로 안내돼 있고, 공단 약가 협상 60일, 건정심 심의 및 복지부 고시 30일 등으로 제도가 설계돼 있지만, 실제 등재 기간은 이와 상당한 차이를 보였다고 지적했다.
특히 항암제는 식약처 허가 이후 건강보험 등재까지 평균 659일(약 1년 10개월)이 소요됐으며, 희귀질환 치료제는 허가 이후 등재까지 3년 10개월이 걸린 사례도 확인됐다고 밝혔다. 연합회는 이 기간 환자들이 허가된 치료제가 있어도 상당 기간 고액 비급여 치료 여부를 결정해야 하는 상황에 놓인다고 설명했다.
단계별로는 항암제의 경우 식약처 허가 이후 건강보험 등재 신청까지 평균 191일(약 6개월)이 소요된 것으로 분석됐다. 연합회는 "제약사가 허가 이후 신속하게 등재 신청을 하지 않으면 등재 절차가 지연돼 환자 피해로 이어진다"고 주장했다.
등재 신청 이후에는 암질환심의위원회 심의·통과까지 평균 156일(약 5개월), 암질환심의위 통과 후 약제급여평가위원회 평가·통과까지 평균 201일(약 6~7개월)이 걸려, 신청 후 두 절차에만 약 1년이 소요된 것으로 나타났다고 설명했다.
정부가 최근 약가제도 개편방안을 발표하며 2026년부터 희귀질환 치료제의 등재 기간을 현행 최대 240일에서 100일 이내로 단축하는 '희귀질환 치료제 신속등재-사후평가 제도' 시범사업을 추진하고, 혁신 신약에는 신속등재-후평가·조정 트랙을 중장기 과제로 추진하겠다는 방향을 제시한 것과 관련해, 연합회는 정책 실효성을 위해 성과 기반의 정교한 사후평가 및 관리 체계가 중요하다고 밝혔다.
연합회는 제도 개선과 함께 제약사의 역할도 필요하다고 덧붙였다. "분석 결과에서도 식약처 허가 이후 제약사의 등재 신청이 늦어지거나 자료 보완이 반복되며 전체 절차가 지연되는 사례가 확인됐다"며 "제약사가 식약처 허가 이후 신속한 등재 신청, 합리적인 약가 수용, 성실한 자료 제출로 환자의 치료 접근성을 높이는 데 적극 나서야 한다"고 주장했다.
연합회는 "암·희귀질환 환자가 치료제를 기다리는 시간이 치료 기회를 잃는 시간이 되어서는 안 된다"며 정부가 환자의 생명과 치료 시기를 최우선으로 하는 신속등재-사후평가 관리체계를 조속히 마련하고 실효성 있게 운영해야 한다"고 촉구했다.

