알테오젠, 고용량 아일리아 제형 기술 국제특허 출원
삼천당, 특허 회피 '제형' 개발 완료…`28년 허가 목표

습성 연령 관련 황반변성 치료제 '아일리아(성분 애플리버셉트)'의 저용량(2㎎) 바이오시밀러 출시에 이어 고용량(8㎎) 제품을 신속히 개발하기 위한 제형 특허 회피 전략이 활용되고 있어 주목된다.
알테오젠은 지난 2일 고용량 '아일리아(성분 애플리버셉트)' 바이오시밀러 개발에 대응 가능한 제형 기술의 국제특허(PCT)를 출원했다고 2일 밝혔다.
회사는 작년 9월 유럽연합 집행위원회(EC)로부터 아일리아 바이오시밀러 제품인 '아이럭스비'의 품목허가를 획득했다. 이 허가로 아이럭스비는 아일리아와 마찬가지로 △습성 연령관련 황반변성(wAMD) △망막 정맥폐쇄성 황반부종(BRVO/CRVO) △당뇨병성 황반부종(DME) △근시성 맥락막 신생혈관(myopic CNV) 등의 적응증에서 처방되고 있다. 다만 아직 한국과 미국 규제기관으로부터 허가는 획득하지 못한 상황이다.
회사 측은 아직 고용량 제품 개발을 착수 또는 결정한 것은 아니지만, 이번 제형 기술 국제특허 출원으로 향후 고용량 제품 개발의 가능성이 열린 점에 의미가 있다는 입장이다.
이 관계자는 "이번 특허 출원이 아일리아 고용량 시밀러 개발과 직접적인 연관이 있는 건은 아니지만, 다양한 농도 범위의 약물을 투여할 수 있는 제형 기술인 만큼 향후 고용량 제품 개발을 결정하게 된다면 이를 활용할 수 있을 것으로 보인다"고 설명했다.
아일리아 고용량의 제형 특허 만료 시점은 유럽을 기준으로 2039년 5월로 알려져 있다. 알테오젠은 저용량 품목허가가 타 시밀러 개발사에 비해 비교적 늦었던 만큼, 고용량 특허 만료일 이전 이를 회피할 수 있는 신규 제형 기술을 개발해 빠른 시장 선점을 노리는 전략을 택한 것으로 보인다.
비슷한 전략을 택한 회사로 삼천당제약이 있다. 회사는 2024년 6월 17일 공시를 통해 자사주 50만주(당시 약 609억원)를 매각해 아일리아 고용량 바이오시밀러와 경구용 GLP-1 제제 개발을 위한 글로벌 임상 비용 및 생산설비 투자에 활용한다고 밝힌 바 있다.
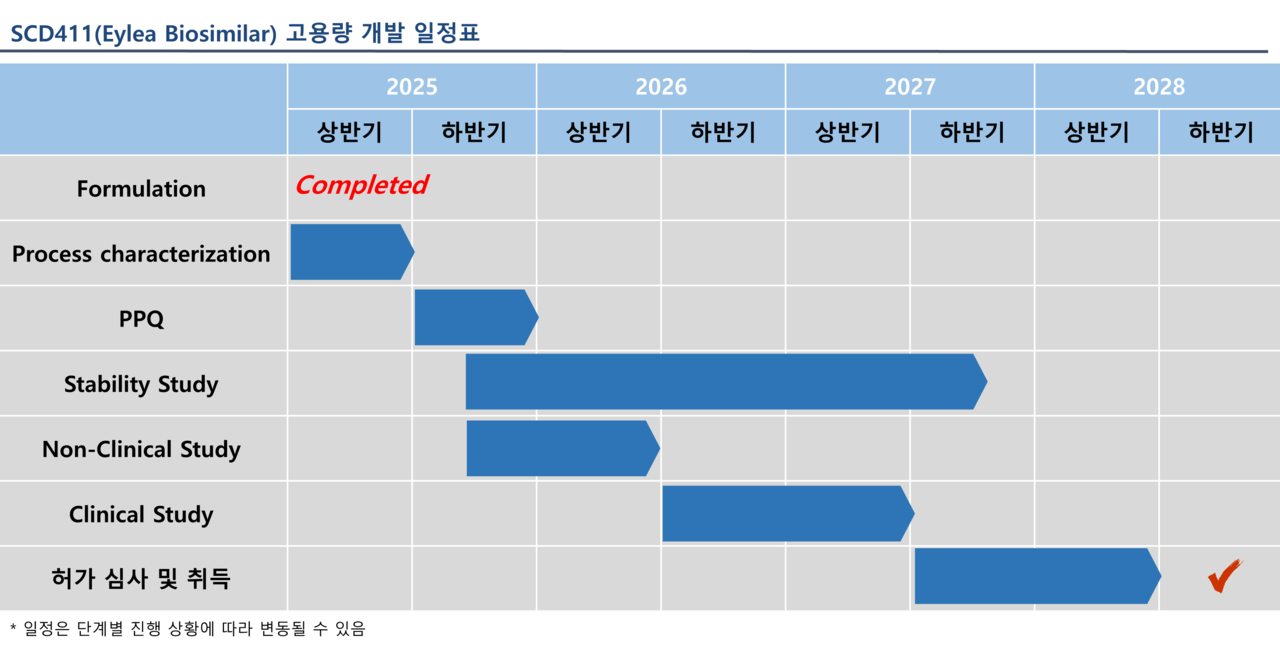
회사는 당시 고용량 아일리아 판매가 시작된 이후부터 글로벌 황반변성 치료제 시장의 규모가 더욱 가중될 것이라고 내다봤다. 지난 2월 진행된 기업소개(IR)에서는 이에 대비하기 위한 시장 전략의 중요성을 강조했고, 고용량 제형특허 회피를 위한 '제형(Foumulation)' 개발을 완료한 상태로 2039년 제형특허 만료 전 조기 시장 진입이 가능하다고 밝힌 바 있다.
더불어 경쟁사보다 낮은 원가로 가격 경쟁력을 강화하겠다고 선언했는데, 이 전략은 작년 12월부터 국내 급여 적용된 회사의 아일리아 시밀러 '비젠프리(연구 물질명 SCD411)'에서도 잘 드러난다. 비젠프리는 국내 경쟁 시밀러 제품 중 가장 높은 약가를 가진 셀트리온의 아이덴젤트 대비 14만원가량 저렴한 19만8000원으로 설정됐다.
회사는 올해 상반기까지 비임상시험을 마치고, 하반기부터 임상시험에 돌입할 예정이다. 2027년 하반기부터 인허가 절차를 진행해 2028년 하반기에는 품목허가를 획득한다는 계획이다.
한편 2024년 자사 저용량 아일리아 바이오시밀러 제품을 출시했던 삼성바이오에피스와 셀트리온은 아직 구체적으로 고용량 개발 계획을 밝히고 있지 않은 상황이다.
한 회사 관계자는 "저용량 아일리아 시밀러 제품의 판매가 본격 궤도에 오르기 시작했다. 한동안은 저용량 제품에 주력할 예정"이라며 "아직 아일리아 고용량 제품이 개발 및 판매된 지 얼마 지나지 않은 만큼, 고용량 시밀러 개발 추진과 관련된 구체적인 계획은 없는 상황"이라고 전했다.

