미 의회 자문기구 "중국 바이오제약, 3년 내 미국 추격 가능"

미국 의회 자문기구가 중국 바이오제약 산업의 급부상을 경고하며 2040년에는 중국 의약품이 미국 FDA 허가의 35%를 차지할 수 있다는 전망을 내놨다.
한국바이오협회 바이오경제연구센터는 22일 이 같은 내용을 담은 이슈 브리핑을 통해 미국 의회 자문기구인 신흥 바이오기술 국가안보위원회(NSCEB) 보고서를 소개했다. NSCEB는 바이오기술 분야에서 미국의 글로벌 리더십 유지를 목표로 한시적으로 운영되는 초당적 자문기구로, 의회와 연방정부에 정책 권고를 제시한다.
NSCEB는 지난 4월 의회에 제출한 보고서에서 중국이 지난 20년간 바이오기술을 국가 전략 우선순위로 삼아 빠르게 성장했으며 미국이 향후 3년 내 신속한 대응에 나서지 않을 경우 회복하기 어려운 격차가 발생할 수 있다고 경고한 바 있다.
당시 보고서는 바이오기술과 바이오제조 역량 강화를 위해 향후 5년간 최소 150억달러를 투자해 민간 자본 유입을 확대해야 한다는 권고를 포함해 6대 원칙과 49개 정책 제안을 제시했다.
이어 NSCEB는 지난 19일 추가 보고서를 통해 중국이 바이오제약 가치사슬 전반을 장악하고 있으며 미국을 따라잡는 데 걸리는 시간이 3년 수준으로 단축됐다고 분석했다.
보고서에 따르면 중국은 지난 10년간 임상시험 규제를 전면 개편해 승인 절차를 대폭 단축했다. 특히 2018년 도입된 '묵시적 승인(implied approval)' 제도로 규제 당국이 정해진 기간 내 반대하지 않으면 임상이 자동 개시되도록 하면서, 과거 1년 이상 소요되던 절차를 크게 개선했다.
중국 바이오기업의 글로벌 위상도 빠르게 변화하고 있다는 분석이다. 2022년에는 중국 기업이 선불금 5000만달러 이상을 받은 글로벌 라이선스 계약 비중이 5%에 불과했으나, 2025년 1분기에는 42%까지 상승했다. NSCEB는 다국적 제약사들이 중국산 의약품 지식재산권 확보를 위해 수억~수십억달러 투자를 준비하는 흐름이 최근 뚜렷해지고 있다고 지적했다.
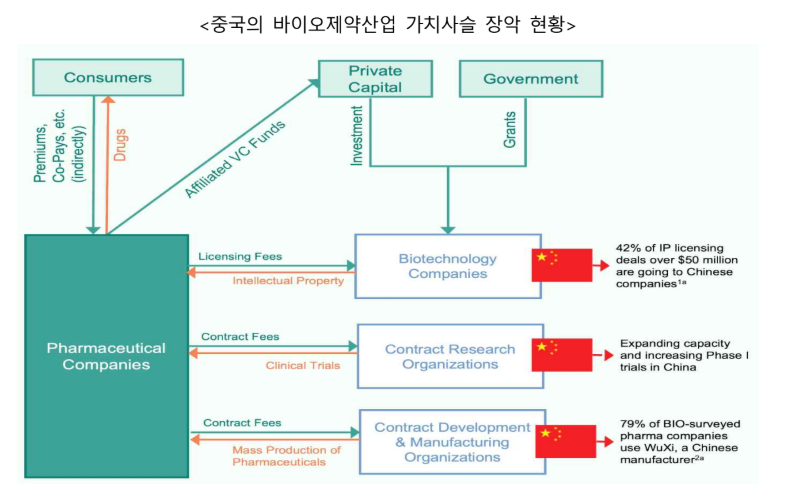
보고서는 이러한 추세가 지속될 경우 2040년까지 중국 의약품이 미국 식품의약국(FDA) 허가의 35%를 차지할 것으로 전망했다. 임상시험 측면에서도 2024년 중국은 세계보건기구(WHO) 국제 임상시험 등록 데이터베이스에 7100건 이상의 임상시험을 등록해 약 6000건을 기록한 미국을 앞섰다.
NSCEB는 사례로 중국 바이오기업 3SBio를 제시했다. 화이자는 올해 초 3SBio의 PD-1/VEGF 이중특이항체 후보물질에 대해 중국 외 권리를 확보하며 선불금 12억5000만달러를 포함해 총 60억달러 이상을 지급하기로 계약했다. 위원회는 이 거래가 중국 기업들이 단순 제조를 넘어 글로벌 제약사가 주목하는 혁신 자산을 창출하고 있음을 보여주는 사례라고 평가했다.
NSCEB는 "미국 정부가 자국 바이오산업을 촉진하는 정책을 채택하지 않을 경우, 중국의 경쟁 우위는 극복하기 어려운 격차로 확대될 수 있다"고 경고했다.

