한국, 프리미엄 있으나 제도 경직성으로 신약 가치 인정 어려워
혁신신약을 대하는 대한민국 정부의 속마음
[끝까지HIT 8호] 건강보험 당국은 '혁신신약에 대한 환자 접근성 강화'를 정책 목표로 줄곧 내세워 왔다. 그러나 정작 공급 및 수혜 당사자인 기업과 환자들은 정부의 목표 실행 의지에 회의적이다. 과거보다 접근성이 개선된 것은 인정하면서도 여전히 간극이 크고, 무엇보다 혁신신약 가치에 대한 반영이 제대로 이뤄지지 않는다는 의견이다. 물론 최근 정부가 업계와 머리를 맞대고 논의한 끝에 혁신가치 보상안을 내놓았지만 해당 제도의 실효성에는 의문을 표한다. 업계의 우려처럼 한국은 혁신신약 도입의 두세번째 옵션으로 전락할 것인지, 환자들은 우회로에서 치료의 기적을 찾아 계속 헤매야 하는지 그 해답을 추구하는 것은 어려운 일이다. 대신 신약과 접근성, 이 두 단어의 거리가 왜 생각만큼 좁혀지지 않는지 그 연원을 찾아본다. [편집자주]
① 신약과 환자 사이, 얼마나 가까워졌나
② 기고 | 고수경 김앤장법률사무소 전문위원
③ 글로벌 제약 MA·GM이 말하는 코리아 패싱
④ 영국 프랑스 캐나다 등 해외 국가 신약 혁신보상 제도

혁신성의 가치를 어떤 수준에서 어떻게 인정할 것이냐가 신약의 약가 문제를 놓고 벌어지는 현재의 논란이다. 우리나라는 경제성 평가를 통해 비용효과성을 입증할 경우 약가 프리미엄을 받을 수 있는 구조를 갖고 있으나, 산업계는 제도 운영의 경직성으로 사실상 그 가치를 인정받기 어려운 상황이라고 입을 모은다. 신약에 대한 혁신보상 제도를 운영하고 있는 해외 국가들의 사례를 통해 시사점을 찾아본다. 한국제약바이오협회, 한국글로벌의약산업협회, 건강보험심사평가원 등 자료를 참고했다.
영국

영국은 환자군이 임상적으로 구분되며, 너무 적어서 소수의 병원에 집중돼 있고, 임상 증상이 만성적이고 심각한 신체적 불편을 초래하는 경우, 해당 의약품이 고도로 특화된 치료에 사용될 것으로 예상되며 초고가이며 생애 전주기에 사용될 수 있고 국가 승인 필요가 충분한 경우를 대상으로 혁신신약 제도(HST, Highly Specialized Technology)를 운영하고 있다. 혁신신약 평가 기준은 질환의 특징, 임상적 유용성, 지불가치, 사회적 요구 등이다.
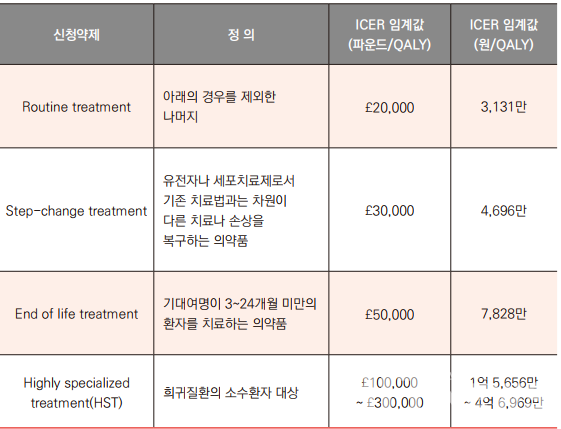
혁신 기술이 반영된 의약품 및 의료기술을 신속하게 수용하기 위한 '혁신 제품 수용 기구(AAC, Accelerated Access Collaborate)'도 눈여겨볼 만하다. 보건의료평가기구(NICE)에서 AAC 제품 선정 및 평가를 진행하며, 선정된 혁신 제품은 여러 프로그램을 통해 지원받을 수 있다. 그 중 '신속 도입 제품(RUP, Rapid Uptake Product)'은 NICE 승인 당시 혁신성을 인정받았으나 도입이 느린 품목에 대해 신속하게 환자들에게 공급될 수 있도록 맞춤형 지원을 시행한다. 특히 임상 근거 수준의 근본적인 한계 와 모형에서의 가정과 변수의 불확실성 을 고려해 ICER 임계치를 다르게 적용하고 있다는 점은 우리나라에 시사하는 바가 크다.
프랑스

프랑스는 약제의 혁신성 가치를 평가해 의약품 등재 및 사후관리에 반영하고 있으며 신약의 부가적 임상 가치(ASMR, Clinical Added Value)를 5개의 등급으로 구분해 평가한다. ASMR 평가 결과는 최초 등재 약가 설정 시 고려되며 사용량-약가 연 동제(PVA)를 포함한 다양한 사후 관리 에 반영해 환급 면제 등 혜택을 제공한다.
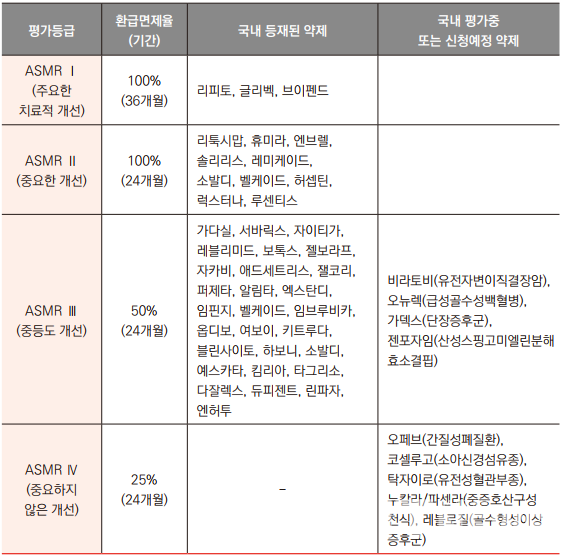
ASMR 1~3 약제 또는 △효과 측면에서 우월성이 있는 경우 △대체약제수의 불충분으로 인한 의학적 수요가 있는 경우 등 요건을 충족하는 ASMR 4 약제는 독일, 영국, 이탈리아, 스페인 등 유럽 주요 4개국(EU price)의 최저가 이상을 받을 수 있다. 또 ASMR 1~3 약제는 표시가(face value price) 및 실제가(net price)를 5년 간 유지할 수 있고 EU price를 수용할 경우 패스트트랙을 적용해 15일 이내 보험 급여가 되도록 운영 중이다
독일

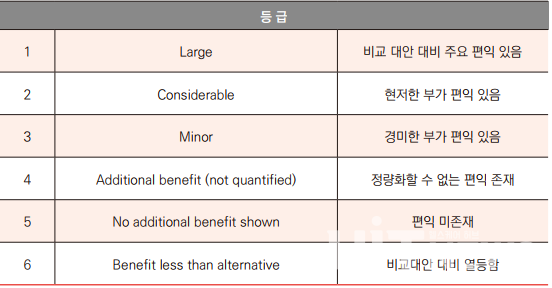
독일은 자율 가격제 를 실시하고 있어 제약사가 원하는 가격으로 신약을 출시할 수 있으며 협상을 통해 환급률과 할인율을 결정한다. 혁신신약에 해당하는 G-BA에서 1~4 등급 의약품의 경우 참조가격제의 적용을 받지 않고 정부와 환급률 및 할인율 을 협상할 수 있는 혜택이 있다. 신약의 치료적 편익을 사망률(Mortality), 이환율(Morbidity), 삶의 질(Health-related quality of life) 등 환자 기반 성과를 바탕으로 결정하며, 총 1~6등급(Large, Considerable, Minor, Additional benefit, No additional benefit shown, Benefit less than alternative)으로 나눠 평가한다. 혁신성 수준과 함께 필수적으로 사용량도 함께 고려해 환급률과 할인율을 협상한다. 특히 희귀의약품이며 보험재정 지출 금액이 연간 3000만 유로 미만인 경우 의무 제출 사항인 비용편익보고서 일부를 면제받음으로써 환급 및 할인에서 일부 혜택을 받는다.
캐나다

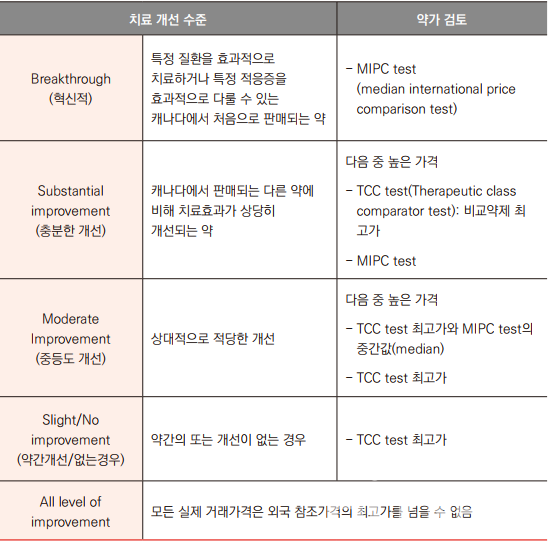
캐나다는 치료적 개선 수준(scientific review)에 따라 신약 을 4가지 등급(Breakthrough, Substantial improvement, Moderate improvement, Slight/No improvement)으로 분류하며 개선 수준이 높을수록 높은 약가로 검토된다. 혁신 의 약품의 경우 영국, 프랑스, 독일, 이탈리아, 스위스, 스웨덴, 일본, 호주, 벨기에, 네덜란드, 노르웨이, 스페인 등 11개국 중앙값을 상한값으로 설정해 검토한다. 이와 함께 주정부와 제약사간 사용량 등에 따라 리베이트(환급) 계약을 진행하고 추후 제약사가 비용을 환급하는 기전이 있다.
일본

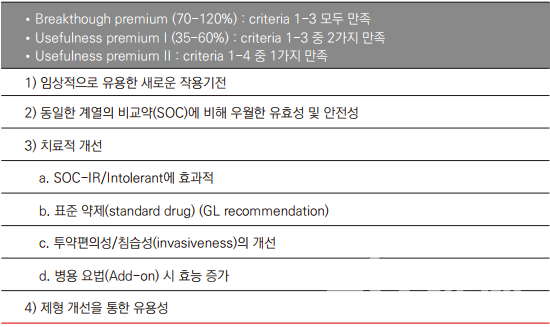
일본은 혁신성이 충분히 약가에 반영될 수 있도록 다양한 가산을 적용하는데 유사약이 없는 신약의 경우 외국 평균 가격 조정을 통해 약가를 결정한다. 유사약이 존재하고 신규성이 있는 신약은 제약사가 제출한 임상시험 자료를 근거로 치료의 개선 정보를 계산해 점수를 차등 부여한다.
벨기에

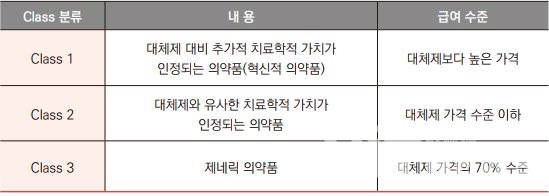
벨기에는 치료학적 가치에 따라 신약을 Class 1, 2, 3으로 분류하고 Class에 따라 약가를 차등적으로 적용한다. Class 1 의약품은 추가적 치료가치가 반영돼 대체제보다 높은 가격수준으로 급여되며, Class 2 의약품은 대체제의 가격수준을 초과할 수 없으며 Class 3 의약품은 대체제보다 약 30% 낮은 수준으로 급여된다. 이처럼 혁신적 의약품의 경우, 초기 약가를 높게 설정한 후 사후관리를 통해서 추후 인하하는 구조를 가지고 있다.
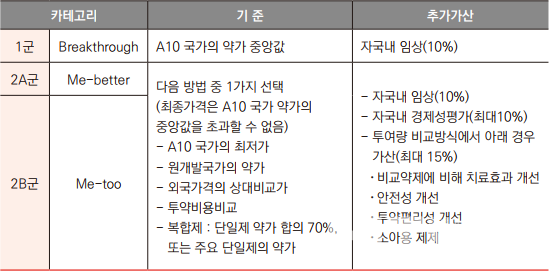
대만

대만은 신약의 임상적 가치 개선 및 혁신 수준을 고려해, 1군(Breakthrough), 2A군(Me-better), 2B군(Me-too) 의약품으로 구분해 약가를 산정한다.