보건산업진흥원, 28일 2025년 첨단제약바이오 개발 인허가 워크숍
이지은 박사 "FDA 미팅 전, 물질 이해ㆍ사업환경ㆍ허가트랙 고민해야"
"'대리 평가변수', '바이오마커' 적합성 FDA 통해 IND 전 미리 확인할 것"

미국 식품의약국(FDA)의 신약 가속승인을 받기 위해서 속도전 못잖게 전략적 소통이 더 핵심이라는 조언이 나왔다. 초기 임상 단계부터 FDA와 긴밀히 대화하며 타깃·기전·평가변수 등 근본적 근거를 마련해야만 가속승인 가능성을 높일 수 있다는 것이다.
28일 서울 성공회의소에서 개최된 '2025년 첨단제약바이오 개발 인허가 워크숍'에서 전(前) FDA 심사관이자 의약품 인허가 컨설팅 업체 아레테볼로(AreteVolo)의 이지은 박사는 FDA 가속승인을 목표로 의약품을 개발하고 있는 기업들이 알아야 할 임상개발 성패를 가르는 초기 전략을 공유했다.
이지은 박사는 FDA와 논의를 시작하기 전에 반드시 △과학적&임상적 근거 △사업 환경(경쟁자&시장 포지셔닝) △규제 경로 등에 대한 근본적인 고민은 마쳐야 한다고 강조했다.
특히 ①현재 개발 중인 물질의 생물학적 타깃, 작용기전(MoA), 노출(Exposure), 결과(Outcome) 등을 뒷받침할 수 있는 데이터를 보유하고 있는지? ②해당 물질이 미충족 수요(Unmet needs)를 해결할 수 있는지? ③임상시험의 평가변수를 선택하고, 연구의 통계적 검정력을 산출할 수 있는 자연사(natural history) 데이터가 있는가? ④확증 임상(pivotal trial)에서 대조군이 존재하는가? 등에 대한 답변이 마련되지 않으면 효과적으로 FDA 논의가 진행되지 못할 것이라는 의견이다.

이 박사는 "일부 기업들은 초기 임상만을 마치고 기술이전(L/O)을 할 것이라는 이유로, 피보탈 임상까지 사전에 디자인할 필요는 없다고 생각한다. 당장 임상시험계획 승인 신청(IND)을 넘어갈 수 있을 지만 생각하고 있는 것"이라면서 "피보탈 임상까지 고려해 디자인하지 않는다면, L/O에 유리한 데이터 패키지를 만들기 어렵다는 사실을 간과하고 있는 듯하다"고 꼬집었다.
이어 "희귀 질환의 경우는 기승인 치료제 존재 여부도 중요하다. 많은 업체들이 앞선 경쟁 제제와 유사하게 임상시험을 디자인하면 우리도 FDA 승인을 받을 수 있겠다고 생각하지만, 큰 오산"이라면서 "그 여부에 따라 대조군 설정도 달라지고, 실제 임상 현장에서의 미충족 수요도 달라진다. 이런 사항들을 사전에 고민해 두지 않는다면, FDA에 IND를 제출할 준비가 돼 있지 않다고 할 수 있다"고 덧붙였다.

이 외에도 임상 현장에서 환자를 최전선에서 치료하고 있는 주요 의료계 권위자(KOL)의 의견 청취의 중요성에 대해 강조했다.
이지은 박사는 “KOL 없이 신약 개발은 불가능하다고 보면 된다. 오픈 마인드로, 이들을 통해 해당 분야 미충족 수요를 파악하고, 어떤 신약을 개발해야 할 지 아이디어를 얻을 수 있다"면서도 "이들은 치료 전문가지 신약 개발자는 아니라는 점을 명심해야 한다. 이들이 원하는 임상시험 디자인이 아닌, FDA로부터 통과될 수 있는 전략을 짜는 것이 중요할 것"이라고 설명했다.
더불어 FDA와 본격적인 IND 신청 절차를 진행하기 전 FDA와 소통(engagement)을 하고 대리 평가변수(Surrogate endpoint)나 바이오마커(Biomarker) 등에 적합성에 대해 사전 확인 또는 설득의 과정을 거치는 것이 중요한 절차로 꼽혔다.
그는 "RMAT, 패스트 트랙, 혁신의약품(Breakthrough) 지정 등 절차를 활용하는 건 결국 FDA와 자주 소통하고, 더 많은 가이던스를 받겠다는 것이다. 우리나라 기업들은 이런 좋은 기회가 제공되는데도, FDA와 소통하려 하지 않고 단순히 주주들에게 회사의 가치를 알리는 수단으로만 활용하고 있는 점이 안타깝다"며 "내가 원하는 방향으로 신약을 개발하기 위해서 FDA를 설득시키기 위한 목적으로 활용해야 한다. 이 과정없이 회사만의 생각으로 진행하다는 임상시험을 다 마쳤다고 할 지라도 가속승인으로 연결 짓지 못할 뿐만 아니라, 최종 품목허가에서 고배를 맞을 수 있다"고 꼬집었다.
이와 함께 한국 기업의 R&D 전략 기획에 있어 특정 결정권자에 집중된 현재의 논의 구조가 변화하지 않는다면, FDA 진출 성공 가능성은 매우 낮다고 강조했다.
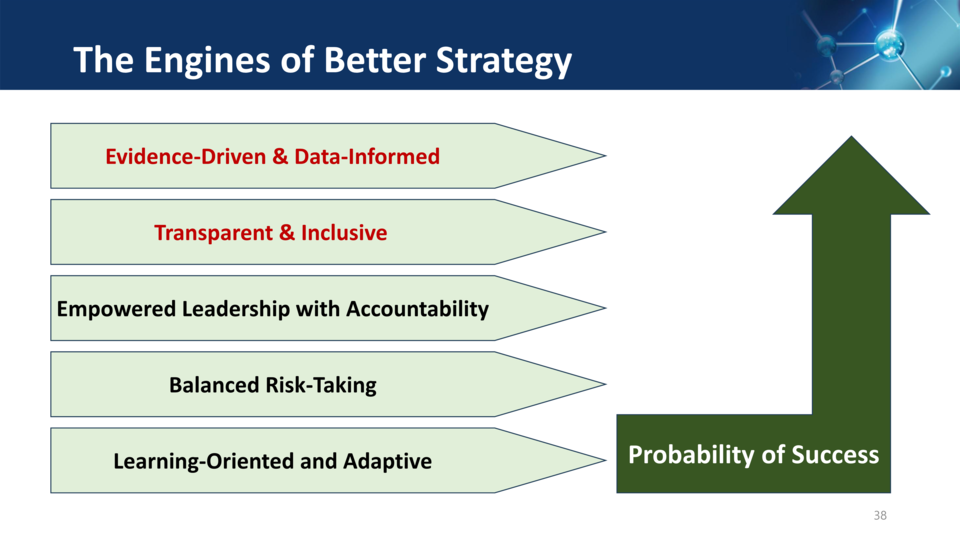
이지은 박사는 "한국 기업들 중 근거에 기반하고(Evidence-Driven), 데이터로부터 답을 찾는(Data-informed) 문화를 제대로 갖추지 못한 곳들이 있다. 논의 과정은 투명해야 하고, 특정 의견에 반대되는 의견을 가진 누군가를 배제하는(non-inclusive) 구조는 건강한 R&D 문화라고 볼 수 없다"며 “이를 개선하는 것이 더 나은 전략을 이끄는 원동력(The engines of better strategy)라는 점을 인지하길 바란다"고 말했다.
한편, 이번 첨단제약바이오 개발 인허가 워크숍은 산업 현장에서 실제로 겪는 과제를 전문가들과 함께 논의하고 해결 방안을 모색할 수 있도록 한국보건산업진흥원이 마련한 참여형 프로그램이다. △실시간 Q&A △라운드테이블 토의 △전문가와의 1:1 컨설팅 등 다양한 참여 방식을 통해, 참가자들이 직접 의견을 주고받으며 발전 방향을 모색할 수 있도록 구성됐다.


예전 인보사 때 보니까 식약처가 안달이 나서 통계적 유의성만으로도 허가 해줘야 한다고 설치더니...
심지어 인보사때는 리스크 베네핏도 고려했었음. 네셀은 리스크 베네핏 좀 봐달라고 그렇게 공개적으로 요구해도 그런거 없이 오로지 임상적 유의성 임상적 유의성 임상적 유의성.....ㅁㅊ